Généralités sur les HSV
Classification
Les virus herpes simplex 1 et 2 (HSV-1 et HSV-2) appartiennent à la famille des Herpesviridae et à la sous-famille des Alphaherpesvirinae.
Epidémiologie
La transmission interhumaine des HSV s’effectue par voir orale ou sexuelle. En France, les séroprévalences sont de l’ordre de 60% à 70% pour le HSV-1 et de 10% à 20% pour le HSV-2. On note depuis plusieurs années une diminution de ces séroprévalences, ainsi qu’un décalage de l’infection initiale par le HSV-1 qui n’a plus lieu dans la petite enfance mais plutôt chez les adolescents ou les jeunes adultes.
Physiopathologie
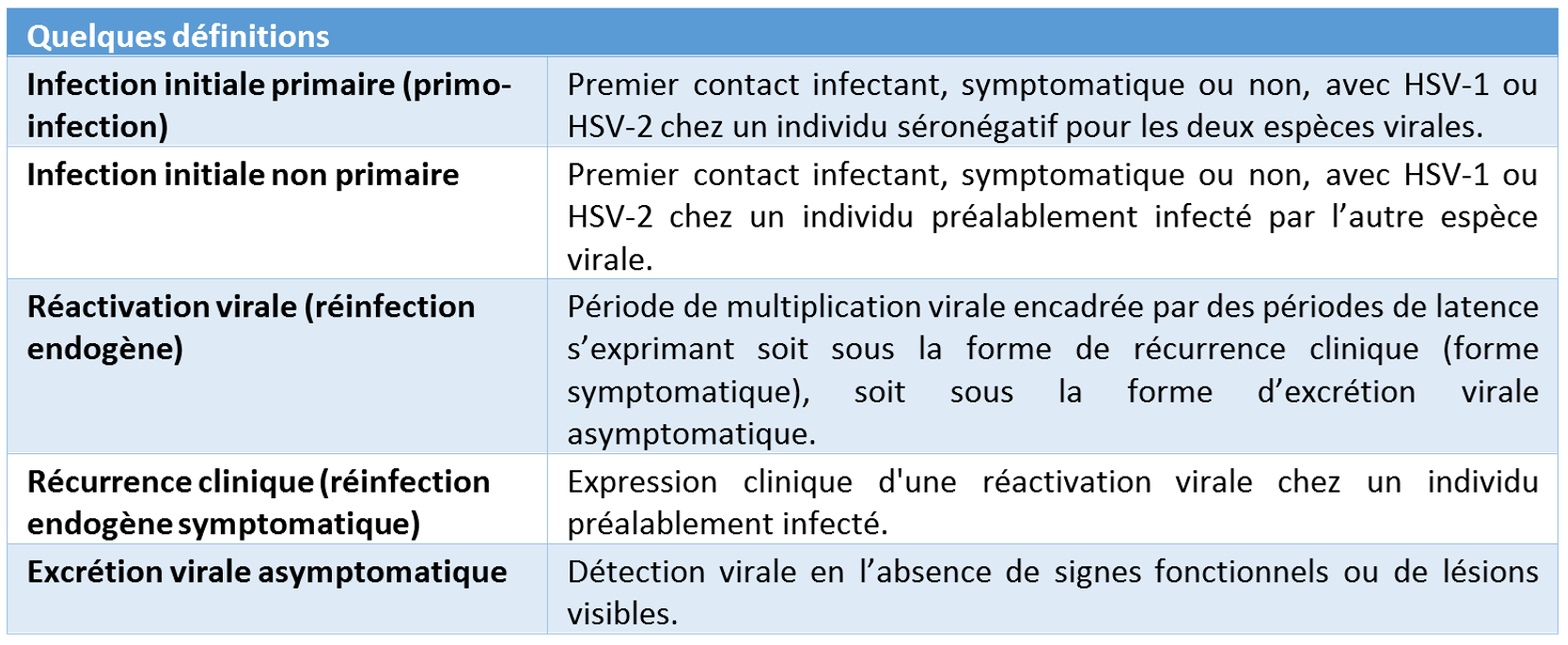
Les HSV sont des virus dermoneurotropes. Suite à l’infection initiale par voie orale ou sexuelle, ces virus persistent à vie chez l’hôte infecté sous forme latente dans les ganglions nerveux sensitifs (ganglions trigéminés ou ganglions sacrés). Les individus infectés sont sujets à des réactivations virales de fréquence variable associées éventuellement à des récurrences cliniques.
Pouvoir pathogène
Les manifestations cliniques des infections par les HSV varient considérablement selon l’âge et le statut immunitaire des patients, selon la nature de l’infection (infection initiale ou réactivation) et selon le virus concerné (HSV-1 ou HSV-2). Chez l’adulte immunocompétent, les infections sont limitées et majoritairement pauci- ou asymptomatiques. A côté des manifestations habituelles de l’herpès oral (HSV-1) et de l’herpès génital (HSV-1 ou HSV-2), des manifestations plus graves peuvent survenir quand certains organes sont touchés (encéphalite, méningite, kératite, uvéite, rétinite, hépatite…) ou chez les individus immunodéprimés (greffe, infection par le HIV…) qui présentent des lésions cutanéomuqueuses sévères, étendues et ulcéro-nécrotiques pouvant se propager aux viscères. Chez les patients hospitalisés en réanimation et sous ventilation mécanique prolongée, le HSV-1 peut être responsable de bronchopneumonie herpétique.
Diagnostic
Le diagnostic direct repose essentiellement sur la détection du génome viral par PCR (prélèvements cutanéomuqueux, génitaux, oculaires, liquide cérébrospinal…). Le statut immunitaire peut-être établi à l’aide de tests sérologiques permettant de détecter les IgG anti-HSV-1 et les IgG anti-HSV-2. En cas d’herpès génital chez la femme enceinte, la combinaison de la PCR (prélèvement génital) et de la sérologie spécifique d’espèce permet de distinguer une infection initiale d’une infection récurrente, ce qui est nécessaire pour la prise en charge.
Traitement antiviral
La prise en charge thérapeutique des infections par les HSV repose sur l’utilisation de l’aciclovir (par voie intraveineuse) ou de sa prodrogue orale, le valaciclovir. En cas d’échec, le foscarnet peut être utilisé en deuxième intention. Ces antiviraux ciblent l’ADN polymérase virale et bloquent la synthèse du génome viral. La prévalence des HSV aux antiviraux est très faible (<1%) chez les individus immunocompétents, à l’exception de ceux souffrant de kératite herpétique récidivante chez qui elle peut atteindre 7%. Elle varie de de 2,5% à 11% les individus immunodéprimés. Au CNR Herpèsvirus, la prévalence de la résistance aux antiviraux chez les patients présentant une infection herpétique et recevant un traitement antiviral depuis au moins 7 jours sans régression significative des lésions a été évaluée au cours de la période 2008-2021 : 46,6% pour le HSV-1 et à 46,4% pour le HSV-2. Il existe de nouveaux antiviraux qui ciblent le complexe hélicase-primase des HSV, l’aménamévir et le pritélivir. L’aménamévir bénéficie d’ores et déjà d’une autorisation d’accès compassionnel pour le traitement des infections sévères par les HSV (dont la kératite herpétique) en situation d’échec, de résistance, d’intolérance ou de contre-indication aux autres antiviraux.
Vaccin
Il n’existe pas de vaccin anti-HSV.