Des études précliniques aux essais cliniques dans les NPIC : Innovations thérapeutiques
A ce jour, la seule prévention reconnue des neuropathies périphériques chimio-induites repose sur le dépistage des neuropathies périphériques préexistantes et/ou la détection précoce de signes de neuropathies chez les sujets soumis à une chimiothérapie neurotoxique. Plusieurs mesures prophylactiques ont déjà fait l’objet d’essais cliniques (administration de calcium/magnésium, de glutathion, de vitamine E…) sans effets significatifs démontrés. Il apparaît évident que prévenir les NPIC par une thérapeutiqu efficace est une priorité pour améliorer la qualité de vie des patients et leur permettre de suivre leur traitement anti-cancéreux de façon optimale.
Neuropathies et SRA
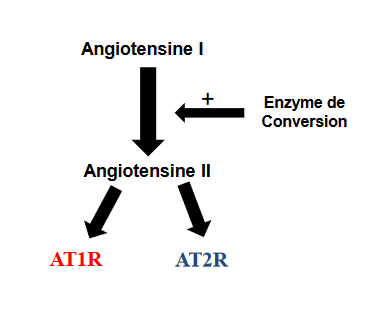
A partir de résultats obtenus sur l’effet du candésartan sur un modèle de neuropathie sensitive pure fonctionnelle induite par la résinifératoxine, les études de l’effet de modulateurs du système rénine-angiotensine (SRA) dans les modèles murins de NPIC ont été développées ces dernières années. Les résultats de ces études précliniques ont permis le démarrage de deux essais cliniques.
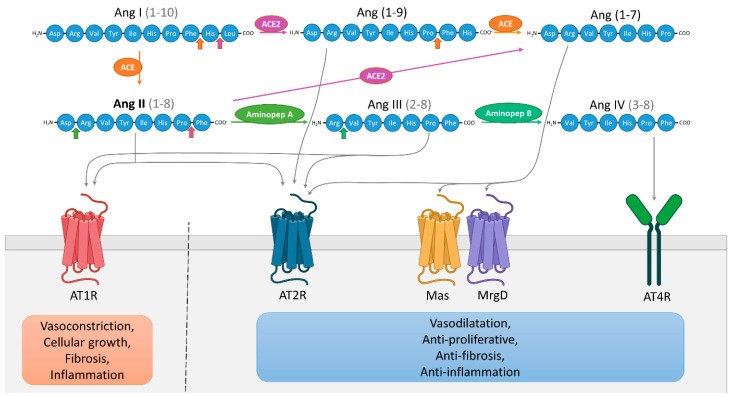
Les récepteurs de l’angiotensine II de type 1 (AT1) et de type 2 (AT2) sont exprimés dans le système nerveux périphérique. Des modulateurs du SRA peuvent, suivant les modèles animaux de douleur, prévenir ou améliorer les dysfonctions de la transmission de la douleur et être neuroprotecteurs et/ou régénérateur. L’étude de l’effet de ces modulateurs sur nos modèles murins de NPIC a donc été effectué.
Modèle NPIV et modulateurs du SRA
Le modèle NPIV a permis de mettre en évidence l’effet neuroprotecteur du candésartan et est à l’origine d’un essai clinique et de nombreuses collaborations industrielles qui se multiplient au fil des années.
Ce travail a également permis le dépôt et l’acceptation d’un brevet interntional avec la laboratoire suédois Vicore Pharma concernant le C21 (ou Buloxibutid) intitulé « Nouvelle utilisation du C21 (et autres agonistes AT2) pour le traitement thérapeutique de la neuropathie périphérique ».
Un essai clinique porté par le Centre de Référence, nommé NEUPERSART (Evaluation de l’apport du candésartant dans la prévention des neuropathies périphériques induites par la vincristine chez des patients traités pour un lymphome B – Etude de phase II randomisée) a également été réalisé. Il est actuellement terminé.
Modulateurs du SRA et neuropathies induites par l'OXA et le PTX
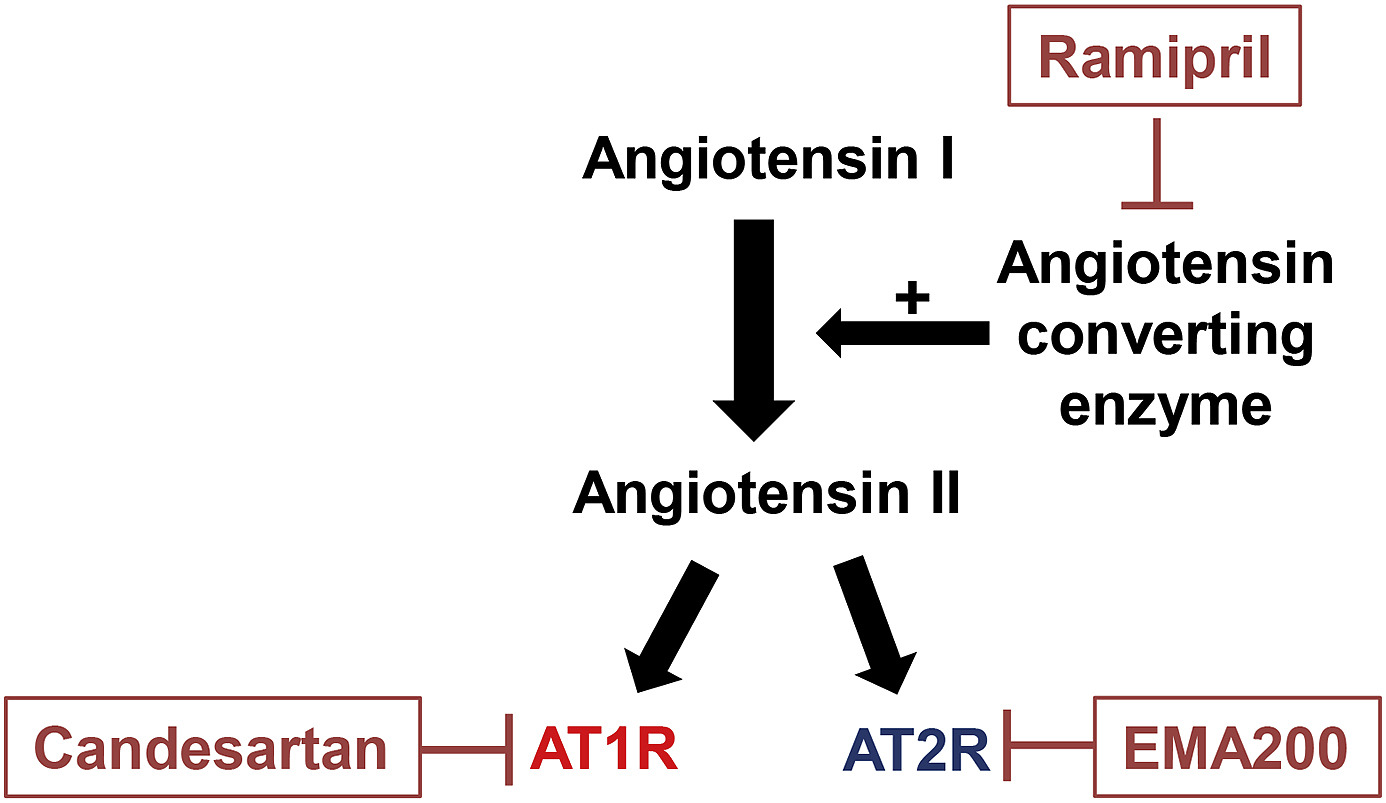
Le modèle de neuroptahie induite par l’OXP (oxaliplatine) a permis de mettre en évidence l’effet neuroprotecteur d’une nouvelle molécule candidate : le ramipril, tandis qu’un effet neuroprotecteur du candésartant n’a pas été constaté.
Ce travail met en évidence deux résultats principaux : (i) l’identification d’autres modulateurs du SRA comme nouvelles molécules neuroprotectrices dans le traitement de la neuropathie périphérique induite par l’OXP, et (ii) la nécessité de l’adaptation du traitement de la prise en charge des effets indésirables neurotoxiques des molécules de chimiothérapies en fonction de l’agent.
Le modèle de neuropathie induite par le PTX a été développé et l’évaluation des effets du ramipril dans la prévention de la NPIP étudiés tout comme l’implication des AT2 dans le rôle neuroprotecteur.
Une étude prospective, OncotoxSRA, a également été menée et est finalisée. Dans celle-ci, 120 patients ont été inclus et suivis depuis le début du programme de chimiothérapie neurotoxique jusqu’à l’évaluation finale. Il a été constaté une sévérité significativement plus faible de la neuropathie dans le groupe inhibiteur du SRA, chez les patients recevant une chimiothérapie à base de platine, mais aucune différence statistiquement significative n’a été retrouvée pour les autres paramètres considérés. Ainsi, pour confirmer le potentiel neuroprotecteur des inhibiteurs du SRA pendant la chimiothérapie, des essais contrôlés randomisés mériteraient d’être menés.
Nouvelles cibles thérapeutiques
Les douleurs neuropathiques associées aux NPIC sont spécifiques à la pathologie de chaque agent anticancéreux neurotoxique et nécessite une prise en charge particulière qui, actuellement, est limitée dans le choix des molécules efficaces disponible sur le marché. En effet, ce fort manque d’options thérapeutiques efficaces dans la prise en charges des douleurs induites par les NPIC est un facteur limitant à un bon suivi du traitement anticancéreux chez un nombre croissant de patients. Il devient donc urgent de développer de nouvelles stratégies thérapeutiques dans la prévention des NPIC.
Une étude approfondie met en avant un autre récepteur qui serait présent dans le système nerveux sensitif et implique son rôle dans la modulation de la douleur : le récepteur à la cholécystokinine de type 2 ou CCK2R. Ainsi, ce récepteur devient une cible prometteuse pour le développement de nouveaux traitements contre la douleur et incite donc à se focaliser sur l’étude de ces modulateurs, tels que le proglumide, le Ly225910 ou encore le Netazepide administrable chez l’Homme puisqu’il est actuellement en essai clinique de phase 2 dans le traitement des tumeurs gastriques endocrines. Pour ce dernier, une collaboration avec le laboratoire Trio Medicines Ltd de Londres est en cours par le biais d’un contrat de type MTA.
Quelques articles représentatifs
– Netazepide, an antagonist of cholecystokinin type 2 receptor, prevents vincristine-induced sensory neuropathy in mice. Bernard et al. Pharmaceuticals (Basel). 2024 Jan 23;17(2):144. PMID: 38399359
– Blockage of cholecystokinin type 2 receptors prevents the Onset of Vincristine Induced Neuropathy in Mice. Bernard et al. Pharceutics. 2022 Dec 16;14(12):2823. PMID : 36559317
– Renin-Angiotensin-System inhibitors for prevention of chemotherapy-Induced Peripheral Neuropathy: OncotoxSRA, a preliminary Cohort Study. Frachet et al. J. Clin Med. 2022 May 23;11(10):2939. PMID: 35629066
– Neuroprotective effect of ramipril is mediates by AT2 in a mouse model of paclitaxel-induced peripheral neuropathy. Bouchenaki et al. Pharmaceutics. 2022 Apr 12;14(4):848. PMID: 35456682
– Ramipril alleviates oxaliplatine-induced acute pain syndrome in mice. Bouchenaki et al. Front Pharmacol. 2021 Jul 19:21:712422. PMID: 34349658
– An overview of ongoing clinical trials assessing pharmacological therapeutic strategies to manage chemotherapy-induced peripheral neuropathy, based on preclinical studies in rodent models. Bouchenaki et al. Fundam Clin Pharmacol. 2021 Jun;35(3):506-523. PMID: 33107619
– The Angiotensin II Type 2 Receptor, a Target for Protection and Regeneration of the Peripheral Nervous System? Danigo et al. Pharmaceuticals (Basel). 2021 Feb 24;14(3):175. PMID: 33668331
– Neuroprotective effect of angiotensin II type 2 receptor stimulation in vincristine-induced mechanical allodynia. Bessaguet et al. Pain. 2018 Dec;159(12):2538-2546. PMID: 30086116
– Candersartan prevents resiniferatoxin-induced sensory small-fiber neuropathy in mice by promoting angitensin II-mediated AT2 receptor stimulation. Bessaguet et al. Neuropharmacology. 2017 Nov;126:142-150. PMID: 28882562